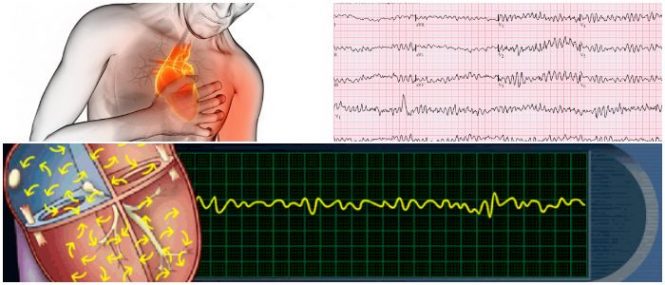
Un ritmo cardíaco que produce un latido cardiaco rápido e inadecuado y pone en peligro la vida.
La fibrilación ventricular (FV) es una arritmia cardíaca potencialmente mortal en la que la contracción coordinada del miocardio ventricular se reemplaza por una excitación desorganizada de alta frecuencia, lo que provoca que el corazón no bombee sangre.
La FV es la arritmia más comúnmente identificada en pacientes con paro cardíaco. En el contexto prehospitalario, el 65-85% de los pacientes en paro cardíaco tienen FV identificada como el ritmo inicial por el personal de los servicios de emergencia. La fibrilación ventricular por lo general termina en la muerte en minutos a menos que se establezcan medidas correctivas inmediatas.
La tasa de supervivencia en el paro cardíaco extrahospitalario ha aumentado con la expansión de los sistemas de rescate de emergencia basados en la comunidad, el uso generalizado de desfibriladores externos automáticos (DEA) y el aumento del número de laicos capacitados en reanimación cardiopulmonar (RCP).
En entornos hospitalarios, la fibrilación ventricular se trata con protocolos de soporte vital cardíaco avanzado (SVCA). El tratamiento a largo plazo puede lograrse con terapia médica o colocación de un desfibrilador cardioversor implantable (DCI).
La corrección quirúrgica de los trastornos subyacentes (p. Ej., Intervención coronaria percutánea, cirugía de revascularización coronaria) también puede estar indicada.
Fisiopatología
La fibrilación ventricular ocurre en una variedad de situaciones clínicas, pero la mayoría de las veces se asocia con la enfermedad arterial coronaria (EAC). La fibrilación ventricular puede ser el resultado de un infarto agudo de miocardio (IM) o isquemia o de cicatrización miocárdica de un infarto antiguo.
La taquicardia ventricular (TV) puede degenerar en FV. La acumulación de calcio intracelular, la acción de los radicales libres, las alteraciones metabólicas y la modulación autónoma son influencias importantes en el desarrollo de la FV durante la isquemia.
El inicio de la FV puede ocurrir de varias maneras.
Por ejemplo, si el miocardio es estimulado por un complejo ventricular prematuro durante la extremidad ascendente de la onda T, el impulso puede propagarse erráticamente a través de las células miocárdicas variablemente refractarias y establecer patrones de reentrada que dan como resultado la despolarización ventricular caótica. En consecuencia, la contracción miocárdica coordinada se interrumpe.
Los patrones de reentrada se dividen en múltiples wavelets más pequeñas y el nivel de desorganización aumenta, con circuitos de reentrada que producen activación de alta frecuencia de las fibras del músculo cardíaco. A medida que el corazón pierde su capacidad de bombear sangre, la isquemia del miocardio empeora y se produce un círculo vicioso autoperpetuante que lleva a la muerte si no se corrige.
En el electrocardiograma (ECG), la fibrilación ventricular se manifiesta como un patrón caóticamente irregular. Este patrón es grueso inicialmente pero se vuelve más fino a medida que aumenta la desorganización ventricular. A medida que la forma de onda del ECG se aplana, la probabilidad de desfibrilación exitosa disminuye.
Etiología
La enfermedad de la arteria coronaria (EAC) es el factor etiológico más común que predispone a los pacientes a la fibrilación ventricular. En los sobrevivientes de paro cardíaco, se observa EAC con estenosis mayor de 75% en 40-86% de los pacientes, según la edad y el sexo de la población estudiada. En los estudios post mortem de personas que han fallecido por FV, la aterosclerosis extensa es el hallazgo patológico más frecuente.
En un estudio de autopsia de 169 casos de muerte coronaria, aproximadamente el 61% de los pacientes habían muerto repentinamente de presunta FV, y otro 15% de los casos mostraba más del 75% de estenosis en 3 o 4 vasos y lesiones graves similares en al menos 2 vasos. Ninguna lesión de la arteria coronaria se asocia con un mayor riesgo de fibrilación ventricular.
Sin embargo, solo aproximadamente el 20% de las autopsias relacionadas con FV han mostrado evidencia de un IM reciente. Una mayor proporción de autopsias (40-70%) muestran evidencia de un infarto de miocardio cicatrizado. Muchos de estos corazones también revelan evidencia de fisuras en la placa, hemorragia y trombosis.
El Estudio de Cirugía de la Arteria Coronaria (CAC) mostró que mejorar quirúrgicamente o restablecer el flujo sanguíneo al miocardio isquémico disminuyó el riesgo de FV, especialmente en pacientes con enfermedad de 3 vasos e insuficiencia cardíaca, en comparación con el tratamiento médico.
Este hallazgo sugiere que la isquemia aguda transitoria es uno de los principales eventos desencadenantes de muerte súbita arrítmica. Se cree que la eficacia de los bloqueadores beta en la disminución de las tasas de mortalidad súbita.
Esto es especialmente cuando se administra a pacientes con infarto de miocardio con fibrilación ventricular, TV y contracciones ventriculares prematuras (CVP) de alta frecuencia, se debe en parte a la capacidad de los betabloqueantes para disminuir la isquemia los bloqueadores beta también aumentan el umbral de fibrilación ventricular en animales isquémicos y disminuyen la tasa de ectopia ventricular en pacientes con IM.
La reperfusión del miocardio isquémico con trombolisis o angioplastia puede inducir inestabilidad eléctrica transitoria por varios mecanismos diferentes. Uno de estos, el espasmo de la arteria coronaria, expone el miocardio a isquemia e insultos de reperfusión.
Los posibles mecanismos del vasoespasmo coronario incluyen factores del sistema nervioso autónomo, especialmente la actividad alfa-adrenérgica; actividad vagal; susceptibilidad del recipiente; y factores humorales, particularmente aquellos asociados con la activación y agregación de plaquetas.
Las anormalidades de las arterias coronarias no ateroscleróticas también se asocian con una mayor incidencia de muerte súbita. Tales anormalidades incluyen lesiones congénitas, embolia, arteritis y anomalías mecánicas, como aneurismas de la arteria coronaria.
Cuando la documentación del ritmo antecedente está disponible, a menudo muestra que la TV rápida precede a la fibrilación ventricular. En pacientes con cardiopatía isquémica crónica, la TV monomórfica derivada de un foco de reentrada es el precursor más común de la FV.
Otros factores asociados con un mayor riesgo de FV incluyen CVP frecuentes, particularmente formas complejas (como CVP multiformes) y otras con intervalos de acoplamiento cortos (fenómeno R-T-T).
Aunque muchos individuos tienen sustratos cardíacos anatómicos y funcionales que los predisponen a arritmias ventriculares, solo un pequeño porcentaje desarrolla FV. La interacción entre la isquemia regional, la disfunción ventricular izquierda (VI) y los eventos incitantes transitorios (p. Ej., Isquemia agravada, acidosis, hipoxemia, tensión de la pared, fármacos, alteraciones metabólicas) se ha propuesto como el precipitador de la FV.
Se estima que el 3-9% de los casos de TV y FV ocurren en ausencia de isquemia miocárdica. Hasta el 1% de los pacientes con paro cardíaco extrahospitalario tienen una fibrilación ventricular idiopática sin una enfermedad cardíaca estructural discernible.
Hasta el 15% de los pacientes menores de 40 años que experimentan fibrilación ventricular no tienen una cardiopatía estructural subyacente. En un estudio de 1993, Belhassen y Viskin notaron que 4 de 11 pacientes con antecedentes de FV y sin cardiopatía estructural tenían anomalías histológicas en la biopsia endomiocárdica.
Epidemiología
Muchos episodios de fibrilación ventricular no son vistos, por lo que es difícil evaluar una incidencia exacta. De los aproximadamente 300,000 casos de MSC que ocurren cada año en los Estados Unidos, hasta un tercio se atribuyen a la FV. Esto representa una incidencia de 0.08-0.16% por año en la población adulta, representando más muertes que por cáncer de pulmón, cáncer de mama o síndrome de inmunodeficiencia adquirida (SIDA).
En los grupos de edad pediátrica y adolescente, la FV ocurre con una incidencia anual de 1.3-8.5 casos por cada 100,000 personas, lo que representa aproximadamente el 5% de todas las muertes en este grupo. La FV suele ser la primera expresión de EAC y es responsable de aproximadamente el 50% de las muertes por EAC. La FV a menudo ocurre dentro de la primera hora después del inicio de un IM agudo o síndrome coronario agudo.
En varios estudios poblacionales, la incidencia de paro cardíaco extrahospitalario en los Estados Unidos se ha observado como un descenso en las últimas 2 décadas, pero la proporción de muertes súbitas por FV en pacientes con EAC no ha cambiado.
Se produce una alta incidencia de FV entre determinados subgrupos de población (p. Ej., Pacientes con insuficiencia cardíaca crónica con fracción de eyección <30%, pacientes en fase convaleciente después de infarto de miocardio, pacientes que sobrevivieron a un paro cardíaco); sin embargo, solo un pequeño porcentaje del total de eventos de FV ocurren en estos pacientes.
Los sobrevivientes de un evento cardiovascular importante tienen un mayor riesgo de fibrilación ventricular en los primeros 6-24 meses después del evento. Hasta el 30% de los sobrevivientes de un paro cardíaco pueden experimentar una FV recurrente durante el primer año posterior.
La frecuencia de FV en otras naciones occidentales industrializadas es similar a la de los Estados Unidos. La incidencia de FV en otros países varía como un reflejo de la prevalencia de EAC en esas poblaciones. Se cree que la tendencia hacia una mayor frecuencia de eventos de FV en los países en desarrollo refleja un cambio en los hábitos dietéticos y de estilo de vida.
Los eventos cardiovasculares, incluida la ECF de la FV (pero no la asistolia), ocurren con mayor frecuencia por la mañana y pueden estar relacionados con un aumento de la agregación plaquetaria. También parece haber un aumento en el número de muertes cardiacas subitas (MCS) durante los meses de invierno.
Causas
Cuando el corazón humano late, los impulsos eléctricos que desencadenan una contracción deben seguir una ruta específica hacia el corazón. Si hay algo mal con la ruta de estos impulsos , pueden ocurrir arritmias o latidos cardíacos irregulares.
Cuando los músculos de las cuatro cámaras del corazón se tensan, se produce un latido cardíaco. Durante un latido del corazón, una cámara se cierra y empuja la sangre.
Durante un latido del corazón, las aurículas musculares o las cámaras superiores más pequeñas se contraen y llenan de sangre los ventrículos relajados.
La contracción comienza cuando el nódulo sinusal, un pequeño grupo de células en la aurícula derecha, emite un impulso eléctrico que hace que las aurículas derecha e izquierda se contraigan.
El impulso eléctrico continúa al centro del corazón, al nodo auriculoventricular. Este nodo se encuentra en la vía entre las aurículas y los ventrículos. Desde el nódulo auriculoventricular, el impulso viaja a través de los ventrículos, lo que hace que se contraigan.
Como resultado, la sangre se bombea desde el corazón hacia el cuerpo.
Síntomas
Los signos más comunes de fibrilación ventricular son un colapso repentino o desmayo, porque los músculos y el cerebro han dejado de recibir sangre del corazón.
Aproximadamente una hora antes de la fibrilación ventricular, algunas personas experimentan:
- Mareo.
- Náusea.
- Dolor en el pecho.
- Taquicardia o latido cardíaco acelerado y palpitaciones.
Pronóstico
Las posibilidades de supervivencia de un evento índice de FV dependen de la reanimación cardiopulmonar (RCP) del espectador, la disponibilidad o llegada rápida de personal y aparatos para desfibrilación y soporte vital avanzado, y el transporte a un hospital.
Aunque los pacientes con paro cardíaco no traumático son más propensos a resucitar con éxito de fibrilación ventricular que de cualquier otra arritmia, el éxito depende mucho del tiempo. La probabilidad de éxito generalmente disminuye a una tasa de 2-10% por minuto.
La desfibrilación temprana a menudo hace la diferencia entre la discapacidad a largo plazo y la recuperación funcional. La colocación de desfibriladores externos automáticos (DEA) en todas las comunidades y la capacitación del público en su uso tiene el potencial de mejorar los resultados de la muerte súbita cardíaca (MSC).
En pacientes que acuden a un servicio de urgencias (SU) después de un episodio de fibrilación ventricular, el pronóstico de morbilidad y mortalidad se puede determinar mediante el cálculo del puntaje de paro cardíaco, desarrollado por Thompson y McCullough.
Este puntaje se basa en la presión arterial sistólica, el tiempo desde la pérdida de la conciencia hasta el retorno de la circulación espontánea y la capacidad de respuesta neurológica. .
Sin embargo, incluso en circunstancias ideales, solo un 20% de las personas que sufren un paro cardíaco fuera del hospital sobreviven hasta el alta hospitalaria.
En un estudio de supervivencia de paro cardiaco extrahospitalario en la ciudad de Nueva York, solo el 1,4% de los pacientes sobrevivieron al alta hospitalaria. Por otro lado, los estudios en áreas suburbanas y rurales han indicado tasas de supervivencia de hasta 35%.
La angiografía coronaria de rutina, con intervención coronaria percutánea (ICP), si está indicada, junto con hipotermia terapéutica leve (temperatura central de 32-34 ° C durante 24 horas), puede alterar favorablemente el pronóstico de pacientes resucitados con hemodinámica estable después de la paro cardíaco en el hospital.
En un estudio retrospectivo de sobrevivientes de paro cardíaco, el 65,6% de los pacientes que se sometieron a una angiografía coronaria temprana sobrevivieron hasta el alta hospitalaria, en comparación con el 48,6% de los que no recibieron la angiografía coronaria.
Un resultado adverso importante de los episodios de fibrilación ventricular es la encefalopatía anóxica, que se produce en el 30-80% de los pacientes. Un estudio realizado en Minnesota sobre todos los sobrevivientes adultos de paro cardiaco relacionado con FV extrahospitalaria entre 1990 y 2008 encontró que los sobrevivientes a largo plazo tenían déficit de memoria a largo plazo.
Tratamiento y gestión
La fibrilación ventricular (FV) aguda se trata de acuerdo con los protocolos de soporte vital cardíaco avanzado (SVCA). Interés en mejorar las tasas de entrenamiento de reanimación cardiopulmonar (RCP) pública, con especial énfasis en el uso de desfibrilación temprana con desfibriladores externos automáticos (DEA) por parte del personal de servicio público (p. , fuego, línea aérea) está muy extendido.
Estas medidas pueden ayudar a lograr los mayores beneficios de salud pública en la lucha contra la muerte súbita. La prevención de la fibrilación ventricular está dirigida a la causa subyacente. La terapia con medicamentos o el tratamiento quirúrgico (p. Ej., Enfermedad arterial coronaria operable) puede ser apropiada en algunos casos, mientras que la ablación por radiofrecuencia es efectiva en una variedad de trastornos.
Los desfibriladores cardioversores implantables (DAI), que proporcionan una desfibrilación temprana de manera efectiva, se usan en pacientes con alto riesgo de fibrilación ventricular recurrente. Los estudios indican que los pacientes con paro de FV que reciben DAI tienen mejores tasas de supervivencia a largo plazo que los pacientes que solo reciben medicación.
Medicación
En la fibrilación ventricular (FV) aguda, se usan medicamentos (por ejemplo, vasopresina, epinefrina, amiodarona) después de 3 intentos de desfibrilación para restaurar el ritmo normal. La amiodarona también puede usarse a largo plazo en pacientes que rechazan un desfibrilador cardioversor implantable (DAI) o que no son candidatos para un DAI.
Sin embargo, no se ha demostrado que la amiodarona sea útil para la prevención primaria de la fibrilación ventricular en pacientes con una fracción de eyección ventricular izquierda (VI) deprimida.
Agentes antiarrítmicos Ia
Los antiarrítmicos de la clase Ia aumentan los períodos refractarios de las aurículas y los ventrículos. La excitabilidad miocárdica se reduce por un aumento en el umbral de excitación e inhibición de la actividad de marcapasos ectópico.
Procainamida (Procanbid, Pronestyl, Pronestyl [SR])
Procainamida es un fármaco de tercera línea de elección para la fibrilación ventricular. Este medicamento generalmente no se recomienda para pacientes con FV, pero debido a su largo tiempo de carga, puede usarse para prevenir recurrencias de la FV o para el tratamiento de la taquicardia ventricular (TV) sostenida.
Agentes antiarrítmicos Ib
Los antiarrítmicos de Clase Ib suprimen la automaticidad del tejido de conducción aumentando el umbral de estimulación eléctrica del ventrículo y el sistema de His-Purkinje e inhibiendo la despolarización espontánea de los ventrículos durante la diástole mediante una acción directa sobre los tejidos.
Los antiarrítmicos de Clase Ib bloquean la iniciación y conducción de los impulsos nerviosos al disminuir la permeabilidad de la membrana neuronal a los iones sodio, lo que resulta en la inhibición de la despolarización, con el consiguiente bloqueo de la conducción.
Lidocaína (Xylocaine, Nervocaine, LidoPen, Duo-Trach)
La lidocaína es un anestésico local y un agente antiarrítmico de clase Ib que aumenta el umbral de estimulación eléctrica del ventrículo, suprimiendo la automaticidad de la conducción a través del tejido. Los agentes de Clase Ib acortan particularmente el potencial de acción. La lidocaína puede probarse en pacientes con TV debido a isquemia.
Agentes antiarrítmicos III
Los antiarrítmicos de clase III prolongan la duración del potencial de acción. Algunos agentes en esta clase inhiben la estimulación adrenérgica (propiedades de bloqueo alfa y beta); afectan los canales de sodio, potasio y calcio; y prolongar el potencial de acción y el período refractario en el tejido miocardial. Estos efectos producen una disminución de la conducción auriculoventricular (AV) y la función del nodo sinusal.
Amiodarona (Pacerone, Cordarone, Nexterone)
La amiodarona es un agente antiarrítmico de clase III indicado para el tratamiento de la FV recurrente potencialmente mortal.
La amiodarona se puede administrar por vía intravenosa u oral.
La fibrilación ventricular recurrente que no se debe a una causa reversible se puede tratar con amiodarona intravenosa (AI). Disminuye la conducción AV y la función del nodo sinusal. También prolonga el potencial de acción y el período refractario en el miocardio e inhibe la estimulación adrenérgica.
La amiodarona también se puede usar por vía oral a largo plazo en pacientes que rechazan los DAI, no son candidatos para DAI o tienen arritmias ventriculares frecuentes.
Agentes antiarrítmicos V
Los antiarrítmicos de clase V tienen un mecanismo de acción diferente del de los agentes de las clases I-IV; en muchos casos, su mecanismo de acción es desconocido.
Sulfato de magnesio
El magnesio actúa como un agente antiarrítmico y disminuye la frecuencia de las contracciones ventriculares prematuras, particularmente cuando es secundario a la isquemia aguda. Los ensayos clínicos no han sido concluyentes en la demostración de su capacidad para mejorar las tasas de mortalidad en el contexto de la FV refractaria.
Vasopresores
Estos agentes aumentan el flujo sanguíneo cerebral y coronario que está presente durante el estado de bajo flujo asociado con el compromiso hemodinámico de la FV.
Epinefrina (Adrenalina)
La epinefrina se considera el fármaco más útil en el paro cardíaco, aunque nunca se ha demostrado que beneficie la supervivencia a largo plazo o la recuperación funcional. La epinefrina estimula los receptores alfa, beta1 y beta2, lo que resulta en la relajación del músculo liso, la estimulación cardíaca y la dilatación de la vasculatura muscular.
Vasopresina (ADH, Pitressin)
La vasopresina es una hormona peptídica que regula la retención de agua del cuerpo al aumentar la absorción de agua en el conducto colector de la nefrona renal. También aumenta la presión arterial al afectar la resistencia vascular periférica.
La vasopresina tiene una indicación no indicada para la fibrilación ventricular que está causando un paro sin pulso. Este agente puede mejorar el flujo sanguíneo de órganos vitales, el suministro de oxígeno cerebral, la capacidad del paciente para ser reanimado y la recuperación neurológica del paciente.
