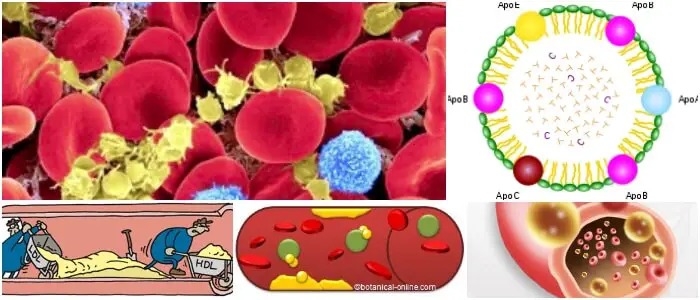
Son partículas de lipoproteína que consisten en triglicéridos (85-92%), fosfolípidos (6-12%), colesterol (1 -3%) y proteínas (1-2%).
El termino «quilomicrones» proviene del griego χυλός, chylos, que significa jugo (de plantas o animales) y micrón, que significa pequeña partícula.
Los quilomicrones son uno de los cinco grupos principales de lipoproteínas:
- Quilomicrones (lipoproteínas de densidad ultrabaja [ULDL, por sus siglas en inglés]).
- Lipoproteína de muy baja densidad.
- Lipoproteína de densidad intermedia.
- Lipoproteína de baja densidad.
- Alta lipoproteína de densidad, que permite que las grasas y el colesterol se muevan dentro de la solución acuosa del torrente sanguíneo.
Los quilomicrones se producen solo en las células intestinales, mientras que las lipoproteínas de muy baja densidad también se sintetizan en el hígado.
Para formar un quilomicrón, los triglicéridos, las vitaminas liposolubles y el colesterol se recubren con una capa de apolipoproteína (tipos de apo A y B), éster de colesterol y fosfolípidos.
Los quilomicrones se producen en el retículo endoplasmático y luego se procesan en el complejo de Golgi donde tiene lugar la glicosilación de la apoproteína.
Se ha sugerido que la apo B está involucrada en el movimiento de quilomicrones desde el retículo endoplásmico al aparato de Golgi, ya que los lípidos se acumulan en el primero en pacientes con abetalipoproteinemia.
Las lipoproteínas de muy baja densidad son más pequeñas que las quilomicrones. Se sintetizan a través de una vía diferente y parecen ser predominantes en los estados de ayuno. Los quilomicrones salen del enterocito por exocitosis.
Aunque son demasiado grandes para atravesar los poros capilares, los quilomicrones y las lipoproteínas de muy baja densidad se cruzan fácilmente en las brechas endoteliales lácteas que están presentes en la fase posprandial.
Los triglicéridos de cadena media se mueven directamente en la circulación portal.
Función
Los quilomicrones transportan los lípidos absorbidos desde el intestino al tejido muscular adiposo, cardíaco y esquelético, donde sus componentes de triglicéridos son hidrolizados por la actividad de la lipoproteína lipasa, permitiendo que los ácidos grasos libres liberados sean absorbidos por los tejidos.
Cuando se ha hidrolizado una gran parte del núcleo de triacilglicerol, se forman remanentes de quilomicrones que son absorbidos por el hígado, transfiriendo así la grasa de la dieta al hígado.
Ácidos grasos Omega-3
Los quilomicrones son las lipoproteínas más grandes y más ricas en triglicéridos de la sangre. Los quilomicrones generalmente están presentes solo en el estado postprandial, debido a que llevan la grasa de la dieta de los intestinos a otros tejidos.
Debido a que se sabe que los ácidos grasos omega-3 reducen significativamente las concentraciones de triglicéridos en ayunas, sus efectos sobre el metabolismo de los triglicéridos posprandiales se han examinado con cierto detalle.
Como era de esperar, el tratamiento con ácidos grasos omega-3 redujo notablemente el aumento de triglicéridos en suero después de una comida rica en grasas.
El efecto no fue el resultado de la mala absorción de los ácidos grasos omega-3, porque las comidas de prueba ricas en aceite de pescado produjeron curvas triglicéridicas postprandiales similares a las grasas de control.
Su efecto en la excursión posprandial de los triglicéridos séricos solo apareció semanas después de la prehidratación con omega-3 Los ácidos grasos y el embotamiento de la trigliceridemia posprandial ocurrieron independientemente del tipo de grasa en la comida de prueba.
Se ha demostrado que la dosis de ácidos grasos omega-3 necesaria para lograr una reducción en la lipemia posprandial es tan baja como 1 g/día.
Hasta el momento se desconoce hasta qué punto la disminución de la lipemia posprandial contribuye a la reducción del riesgo cardiovascular, pero este puede ser un mecanismo por el cual estos ácidos grasos mitiguen el desarrollo de enfermedad coronaria (CHD, por sus siglas en inglés).
Origen
Los quilomicrones se forman en el retículo endoplásmico en las células absorbentes (enterocitos) del intestino delgado. Las vellosidades, revestidas con las microvellosidades del borde en cepillo, proporcionan una gran superficie para la absorción.
Los quilomicrones recién formados se secretan a través de la membrana basolateral hacia los vasos sanguíneos, donde se unen a la linfa para convertirse en quilo. Los vasos linfáticos llevan el quilo al retorno venoso de la circulación sistémica.
A partir de ahí, los quilomicrones suministran al tejido la grasa absorbida por la dieta.
Por lo tanto, a diferencia de los sacáridos y aminoácidos que la digestión libera de los carbohidratos y las proteínas de la dieta (respectivamente), los lípidos de la dieta pasan por alto el sistema portal hepático, lo que significa que el hígado no recibe «primer crack» en ellos.
Etapas
Hay tres etapas en el «ciclo de vida» del quilomicrón:
- Quilomicrón naciente.
- Quilomicrón maduro.
- Restos de quilomicrones.
Quilomicrones nacientes
Los triglicéridos son emulsionados por la bilis e hidrolizados por la enzima lipasa, dando como resultado una mezcla de ácidos grasos y monoglicéridos. Estos luego pasan de la luz intestinal al enterocito, donde se vuelven a esterificar para formar triglicéridos.
Los triglicéridos se combinan luego con fosfolípidos, ésteres de colesterilo y apolipoproteína B-48 para formar un quilomicrón naciente.
Estos son luego liberados por exocitosis de los enterocitos a los vasos sanguíneos laterales, vasos linfáticos que se originan en las vellosidades del intestino delgado, y luego son secretados en el torrente sanguíneo en la conexión del conducto torácico con la vena subclavia izquierda.
El principal componente de la apolipoproteína es la apolipoproteína B-48 (apo B-48).
Restos de quilomicrones
Una vez que se distribuyen las reservas de triglicéridos, el quilomicrón devuelve la apolipoproteína C-II a las lipoproteínas de alta densidad (pero mantiene la apolipoproteína E) y, por lo tanto, se convierte en un resto quilomicrón, ahora solo 30-50 nm.
Catabolismo
Los quilomicrones son demasiado grandes para cruzar la barrera endotelial; por lo tanto, su lipólisis previa a los restos cumple una doble función: transporte de energía a los tejidos y disminución del tamaño para facilitar el catabolismo terminal.
Los experimentos en hepatocitos, hígados de rata perfundidos y más recientemente, estudios de ratones transgénicos y knock-out han demostrado que el transporte remanente de quilomicrones en el hígado está mediado por receptores de la superficie celular.
Aunque existe un consenso general de que la apo E, reconocida por el receptor de lipoproteínas de baja densidad, es el componente de la superficie que dirige los restos de quilomicrones a su sitio de captación.
Se predijo a partir de estudios en sistemas modelo deficientes en receptores de lipoproteínas de baja densidad. Esa eliminación del quilomicrón remanente sería independiente del receptor de lipoproteínas de baja densidad.
Los individuos con hipercolesterolemia familiar homocigótica, que carecen de receptores funcionales de lipoproteínas de baja densidad, no muestran evidencia de un retraso en el aclaramiento de los restos de quilomicrones.
Lo mismo es cierto en un modelo animal para la hipercolesterolemia familiar humana, el conejo hiperlipidémico hereditario de Watanabe.
Además, en estos animales, la infusión intravenosa de apo E disminuye los niveles de colesterol en plasma, lo que respalda la noción de que la apo E media la captación de lipoproteínas a través de las vías independientes de los receptores de lipoproteínas de baja densidad.
Finalmente, la evidencia de un mecanismo separado de eliminación del quilomicrón hepático proviene de estudios en los que se demostró que los factores dietéticos, farmacológicos y hormonales regulan el número de receptores hepáticos de lipoproteínas de baja densidad sin afectar en gran medida la tasa de aclaramiento de los restos de quilomicrones.
Dado que el receptor de lipoproteínas de baja densidad y el receptor remanente quilomicrón propuesto deben compartir al menos una propiedad, concretamente la unión de apo E, los intentos de aislar este receptor se basaron en la supuesta homología de su región de unión a ligando del receptor de lipoproteína de baja densidad.
De hecho, la clonación por homología dio como resultado la caracterización de una proteína de membrana inusualmente grande, compuesta exclusivamente por elementos estructurales encontrados en la molécula de receptor de lipoproteína de baja densidad.
Por lo tanto, se ha denominado proteína relacionada con el receptor de lipoproteínas de baja densidad.
Contiene (entre otros elementos estructurales encontrados en el receptor de lipoproteínas de baja densidad) 31 repeticiones del tipo que forma el dominio de unión del ligando en el receptor de lipoproteínas de baja densidad y 22 repeticiones del factor de crecimiento tipo (A, B y C).
La proteína de membrana inusualmente grande se une a las lipoproteínas de manera dependiente de la apo E, y es sensible al equilibrio entre apo Cs y apo E.
Poco después de su clonación, la proteína relacionada con el receptor de lipoproteína de baja densidad demostró ser idéntico al receptor de la α2-macroglobulina, una proteína plasmática principal que funciona en la «captura» y, por lo tanto, en la inactivación de las proteasas celulares que han entrado en el compartimento plasmático.
Desde entonces, se han identificado muchas más proteínas del complejo plasmático y complejos proteicos que, al menos in vitro, se unen a las proteínas relacionadas con los receptores de las lipoproteínas.
Lo que indica que la proteína relacionada con el receptor de lipoproteína puede desempeñar múltiples funciones en la eliminación de vehículos transportadores de lípidos y de proteinasas potencialmente dañinas.