Es una condición en la que una región del cuerpo se ve privada de un suministro adecuado de oxígeno a nivel del tejido.
La hipoxia puede clasificarse como generalizada, afectando a todo el cuerpo, o local (tisular), afectando una región del cuerpo.
Aunque la hipoxia suele ser una afección patológica, las variaciones en las concentraciones de oxígeno arterial pueden ser parte de la fisiología normal, por ejemplo, durante el entrenamiento de hipoventilación o el ejercicio físico extenuante.
La hipoxia difiere de la hipoxemia y la anoxemia en que la hipoxia se refiere a un estado en el que el suministro de oxígeno es insuficiente, mientras que la hipoxemia y la anoxemia se refieren específicamente a estados que tienen un suministro de oxígeno arterial bajo o nulo.
La hipoxia en la que hay una privación completa del suministro de oxígeno se conoce como anoxia.
La hipoxia generalizada ocurre en personas sanas cuando ascienden a grandes altitudes, donde causa el mal de altura que conduce a complicaciones potencialmente fatales: edema pulmonar a gran altitud (HAPE, por sus siglas en inglés) y edema cerebral a gran altitud (HACE, por sus siglas en inglés).
La hipoxia también ocurre en individuos sanos al respirar mezclas de gases con un bajo contenido de oxígeno, como por ejemplo, mientras se sumerge bajo el agua, especialmente cuando se utilizan sistemas de rebreather de circuito cerrado que controlan la cantidad de oxígeno en el aire suministrado.
La hipoxia intermitente leve y no perjudicial se usa intencionadamente durante el entrenamiento en altitud para desarrollar una adaptación del rendimiento atlético tanto a nivel sistémico como celular.
La hipoxia es una complicación común del nacimiento prematuro en recién nacidos. Debido a que los pulmones se desarrollan al final del embarazo, los bebés prematuros con frecuencia poseen pulmones subdesarrollados.
Para mejorar la función pulmonar, los médicos con frecuencia colocan a los bebés en riesgo de hipoxia dentro de las incubadoras (también conocidas como humidicribs) que proporcionan una presión positiva continua en las vías respiratorias.
Hipoxia local o hipoxia tisular
Si el tejido no se perfunde adecuadamente, puede sentirse frío y pálido; si es grave, la hipoxia puede provocar cianosis, una decoloración azul de la piel. Si la hipoxia es muy grave, un tejido puede llegar a ser gangrenoso. El dolor extremo también se puede sentir en o alrededor del sitio.
La hipoxia tisular por el bajo suministro de oxígeno puede deberse a una baja concentración de hemoglobina (hipoxia anémica), bajo gasto cardíaco (hipoxia estancada) o baja saturación de hemoglobina (hipoxia hipóxica).
La consecuencia de la privación de oxígeno en los tejidos es un cambio al metabolismo anaeróbico a nivel celular. Como tal, la reducción del flujo sanguíneo sistémico puede dar como resultado un aumento de lactato sérico.
Los niveles séricos de lactato se han correlacionado con la gravedad de la enfermedad y la mortalidad en adultos críticamente enfermos y en recién nacidos con ventilación con dificultad respiratoria.
Síntomas de la hipoxia tisular
La hipoxia tisular, debido a la baja tensión arterial de oxígeno, el flujo sanguíneo inadecuado o una combinación de estos dos factores, da como resultado un cambio al metabolismo anaeróbico a nivel celular.
Por lo tanto, un flujo sanguíneo sistémico reducido puede dar como resultado un aumento en el lactato sérico.
Los niveles séricos de lactato se han correlacionado con la gravedad de la enfermedad y la mortalidad en adultos críticamente enfermos y en recién nacidos con ventilación con síndrome de dificultad respiratoria.
El nivel normal de lactato en este grupo de lactantes es inferior a 2.5 mmol/L y existe una asociación con la mortalidad a medida que el nivel de lactato sérico aumenta por encima de este umbral.
Este puede ser un problema muy serio. Jugando la amenaza y la persistencia de la privación de sangre, puede causar inconvenientes físicos, dolor y muerte celular. La sangre traslada oxígeno y nutrientes a las células del cuerpo.
Cualquier baja en el abasto de estas sustancias que sostienen el organismo produce una depreciación en el rendimiento celular y, si es muy serio, deterioro celular que el cuerpo puede o no compensar.
Si la reducción del flujo de sangre y oxigeno es rígida y aguda, se la conoce como isquemia (descrita más adelante) o shock.
Puede ocurrir en cualquier parte del cuerpo como resultado de una variedad de condiciones. Es común en las extremidades, como las manos y los pies, los riñones, la piel y el corazón.
La disminución cognitiva, los trastornos de atención, la depresión, la inestabilidad emocional, los trabajos motores descoordinados, los problemas visuales, auditivos y espaciales (divisar dónde se halla su cuerpo en el espacio y ubicarlo en la posición correcta).
Todo esto es secuela de la depreciación del flujo de sangre a ciertas partes del cerebro.
Puede experimentar hipoperfusión sin darse cuenta, y sin notar que sus habilidades físicas y mentales están reducidas. Aún menos posible es que haga la vínculo entre el dolor y sus capacidades o cambios de humor sutilmente reducidos.
La falta de cuidado y atención a estos signos podrían provocar un aumento de los síntomas y dablemente un mayor peligro de daño serio de las células por dificultades en el flujo sanguíneo a largo plazo.
El síntoma más considerable que podría tener es dolor en el área afectada y/o subyacente. Muchos pacientes meramente optan por vivir con el dolor, y lo aceptan como una parte desafortunada pero normal de la vida.
Ignorar el tratamiento de este dolor podría hacerle daño físico y mental. Posiblemente podría conducir a problemas más graves en el futuro si no se tratan.
Si padece dolor crónico lo mejor que puede hacer por usted mismo es dejar que un experimentado espía profesional lo examine.
Causas
El oxígeno se difunde pasivamente en los alvéolos pulmonares de acuerdo con un gradiente de presión. El oxígeno se difunde desde el aire respirado, mezclado con vapor de agua, a la sangre arterial, donde su presión parcial es de alrededor de 100 mmHg (13.3 kPa).
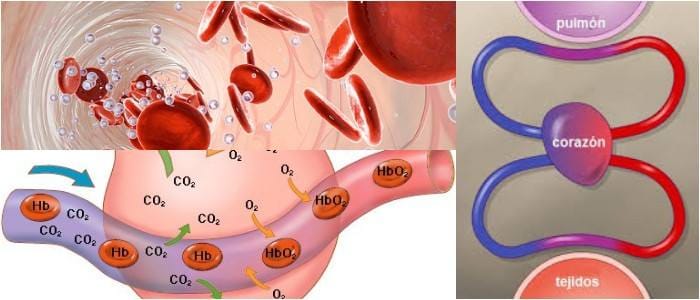
En la sangre, el oxígeno está ligado a la hemoglobina, una proteína en los glóbulos rojos. La capacidad de unión de la hemoglobina está influenciada por la presión parcial de oxígeno en el ambiente, como se describe en la curva de disociación de oxígeno-hemoglobina. Una menor cantidad de oxígeno se transporta en solución en la sangre.
En los tejidos periféricos, el oxígeno nuevamente se difunde por un gradiente de presión hacia las células y sus mitocondrias, donde se usa para producir energía junto con la descomposición de la glucosa, las grasas y algunos aminoácidos.
La hipoxia puede ser el resultado de una falla en cualquier etapa de la administración de oxígeno a las células.
Esto puede incluir presiones parciales disminuidas de oxígeno, problemas con la difusión de oxígeno en los pulmones, hemoglobina disponible insuficiente, problemas con el flujo de sangre al tejido del extremo y problemas con el ritmo respiratorio.
Experimentalmente, la difusión de oxígeno se vuelve limitante (y letal) cuando la presión parcial de oxígeno arterial desciende a 60 mmHg (5.3 kPa) o menos.
Casi todo el oxígeno en la sangre está ligado a la hemoglobina, por lo que interferir con esta molécula transportadora limita el suministro de oxígeno a la periferia.
La hemoglobina aumenta la capacidad de transporte de oxígeno de la sangre aproximadamente 40 veces, con la capacidad de la hemoglobina de transportar oxígeno influenciada por la presión parcial de oxígeno en el ambiente, una relación descrita en la curva de disociación oxígeno-hemoglobina.
Cuando se interfiere la capacidad de la hemoglobina para transportar oxígeno, puede producirse un estado de hipoxia.
Isquemia
La isquemia, que significa flujo sanguíneo insuficiente a un tejido, también puede provocar hipoxia. Esto se llama ‘hipoxia isquémica’.
Esto puede incluir un evento embólico, un ataque al corazón que disminuye el flujo sanguíneo general o un trauma en un tejido que daña. Un ejemplo de flujo sanguíneo insuficiente que causa hipoxia local es la gangrena que ocurre en la diabetes.
Las enfermedades como la enfermedad vascular periférica también pueden provocar hipoxia local. Por esta razón, los síntomas empeoran cuando se usa una extremidad.
El dolor también se puede sentir como resultado del aumento de iones de hidrógeno que conduce a una disminución en el pH de la sangre (acidez) creado como resultado del metabolismo anaeróbico.
Hipoxia hipoxémica
Esto se refiere específicamente a estados hipóxicos donde el contenido arterial de oxígeno es insuficiente. Esto puede ser causado por alteraciones en el impulso respiratorio, como:
Alcalosis respiratoria, derivación fisiológica o patológica de la sangre, enfermedades que interfieren en la función pulmonar que producen una falta de coincidencia entre la ventilación y la perfusión.
También una embolia pulmonar o alteraciones en la presión parcial de oxígeno en el ambiente o en los alvéolos pulmonares, como puede ocurrir en altitud o al bucear.
Envenenamiento por monóxido de carbono
El monóxido de carbono compite con el oxígeno por sitios de unión en moléculas de hemoglobina. Como el monóxido de carbono se une a la hemoglobina cientos de veces más que el oxígeno, puede evitar el transporte de oxígeno.
El envenenamiento por monóxido de carbono puede ocurrir de manera aguda, como con la intoxicación por humo, o durante un período de tiempo, como con el tabaquismo. Debido a procesos fisiológicos, el monóxido de carbono se mantiene a un nivel de reposo de 4-6 ppm.
Esto se incrementa en las áreas urbanas (7-13 ppm) y en los fumadores (20-40 ppm). Un nivel de monóxido de carbono de 40 ppm equivale a una reducción en los niveles de hemoglobina de 10 g/l.
El monóxido de carbono tiene un segundo efecto tóxico, es decir, eliminar el desplazamiento alostérico de la curva de disociación de oxígeno y desplazar el pie de la curva hacia la izquierda.
Al hacerlo, es menos probable que la hemoglobina libere sus oxígenos en los tejidos periféricos. Ciertas variantes anormales de la hemoglobina también tienen una afinidad de oxígeno más alta que la normal, y por lo tanto también son pobres en la administración de oxígeno a la periferia.
Altitud
El mal de altura, también conocido como mareo agudo de montaña (AMS, por sus siglas en inglés), es un efecto negativo a la salud de la altura, causado por la exposición aguda a bajas cantidades de oxígeno a gran altitud.
Se presenta como una colección de síntomas inespecíficos, adquirida a gran altitud o con baja presión de aire, que se asemeja a un caso de «gripe, envenenamiento por monóxido de carbono o resaca».
Aunque síntomas menores como la falta de aire pueden ocurrir a altitudes de 1.500 metros (5.000 pies), el mal de montaña agudo ocurre típicamente por encima de 2.400 metros (8,000 pies). Es difícil determinar quién se verá afectado por el mal de altura.
El diagnóstico se respalda en aquellos que tienen una reducción moderada a severa en las actividades.
El mal de montaña agudo puede progresar a edema pulmonar a gran altitud o edema cerebral a gran altitud, ambos potencialmente mortales, y solo se puede curar mediante un descenso inmediato a una altitud menor o la administración de oxígeno.
El mal de montaña crónico es una condición diferente que solo ocurre después de una exposición prolongada a gran altitud.
Gases respiratorios hipóxicos
El gas de respiración en el buceo puede contener una presión parcial insuficiente de oxígeno, particularmente en el mal funcionamiento de los rebreathers. Tales situaciones pueden llevar a la inconsciencia sin síntomas, ya que los niveles de dióxido de carbono son normales y el cuerpo humano detecta la hipoxia pura deficientemente.
Un problema similar existe al inhalar ciertos gases asfixiantes inodoros.
Los gases asfixiantes reducen/desplazan la concentración normal de oxígeno en el aire respirable, donde la exposición prolongada a este gas respiratorio hipóxico conduce a la pérdida del conocimiento, seguido de la muerte por asfixia con gas inerte (asfixia).
Cuando el nivel de oxígeno desciende por debajo del 19.5% v/v (volumen/volumen), el aire se considera deficiente en oxígeno, donde las concentraciones de oxígeno por debajo del 16% del volumen se consideran altamente peligrosas para los humanos.
Como los gases asfixiantes son relativamente inertes e inodoros, su presencia puede no notarse hasta que el organismo reconozca los efectos del dióxido de carbono en sangre elevado (hipercapnia).
La asfixia con gas inerte puede ser deliberada con el uso de una bolsa de suicidio. La muerte accidental ha ocurrido en casos donde las concentraciones de nitrógeno en atmósferas controladas, o metano en minas, no han sido detectadas o apreciadas.
Otro
La función de la hemoglobina también puede perderse oxidando químicamente su átomo de hierro a su forma férrica. Esta forma de hemoglobina inactiva se llama metahemoglobina y se puede obtener al ingerir nitrito de sodio, así como ciertas drogas y otros químicos.
Anemia
La hemoglobina desempeña un papel importante en el transporte de oxígeno por todo el cuerpo, y cuando es deficiente, puede provocar anemia, lo que causa «hipoxia anémica» si disminuye la perfusión tisular. La deficiencia de hierro es la causa más común de anemia.
Como el hierro se usa en la síntesis de hemoglobina, se sintetizará menos hemoglobina cuando haya menos hierro, debido a una ingesta insuficiente o a una absorción deficiente.
La anemia suele ser un proceso crónico que se compensa con el tiempo por el aumento de los niveles de glóbulos rojos a través de la eritropoyetina regulada positivamente. Un estado hipóxico crónico puede ser el resultado de una anemia mal compensada.
Bacterias
La hipoxia tisular (privación de oxígeno en un tejido) puede ocurrir durante una infección bacteriana como resultado de varios factores.
La inflamación resultante impide que la sangre llegue al sitio de infección y/o la angiogénesis local no sigue el ritmo del consumo de oxígeno por parte de las bacterias en división y la población de neutrófilos infiltrante y en expansión.
Los niveles normales de presión de oxígeno (PO2) se clasifican como normoxia a 15-21% de oxígeno, 110-160 mmHg; hipoxia a <12% de oxígeno, 90 mmHg; y anaerobiosis a <0.01% O2, <5 mmHg.
La presión parcial de oxígeno puede oscilar entre 110 mmHg en los alvéolos y 15 mmHg en el hígado, y la presión parcial del oxígeno depende del sitio del tejido.
Los sitios de heridas, que representan sitios de inflamación e infiltración de células mieloides, varían entre 10 y 20 mmHg, y la hipoxia es una característica de los tejidos que experimentan infecciones bacterianas.
La falta de oxígeno en un sitio de infección afecta significativamente la expresión génica de las células bacterianas y hospedadoras, por lo que es importante estudiar la respuesta a la anaerobiosis por S. aureus para desarrollar nuevas terapias y una mayor comprensión del organismo durante el curso de una infección.
Tratamiento
La hipoxia tisular es el resultado principal de la intoxicación por monóxido de carbono. Por lo tanto, según los datos químicos y fisiopatológicos, el oxígeno es el «antídoto natural».
Para contrarrestar los efectos de las enfermedades a gran altitud, el área afectada debe devolver la presión arterial parcial del oxígeno hacia la normalidad. La aclimatación, el medio por el cual el área afectada se adapta a mayores altitudes, restaura parcialmente la presión parcial de oxígeno a niveles estándar.
Dado que los signos y síntomas clínicos de la toxicidad por monóxido de carbono son inespecíficos, todas las víctimas sospechosas deben tratarse con inhalación de oxígeno inmediatamente después de que se extraiga sangre para determinar el contenido de carboxihemoglobina.
Las respuestas individuales a niveles similares de exposición al monóxido de carbono varían ampliamente, desde la muerte hasta un síndrome de Parkinson, hasta un impacto intelectual leve o moderado.
Por lo tanto, inmediatamente después de asegurar las vías respiratorias y la ventilación adecuada, la administración de oxígeno normobárico es la piedra angular de la terapia, reduciendo la vida media de la carboxihemoglobina de una media de 5 horas (rango de 2 a 7 horas) a aproximadamente 1 hora.
El oxígeno hiperbárico a 2.5 atmósferas lo reduce a 20 a 30 minutos y tiene otros beneficios, al menos en modelos animales.
Por ejemplo, en cerebros de ratas, previene la peroxidación de lípidos y la adherencia de leucocitos al endotelio microvascular cerebral a la vez que acelera la regeneración de la citocromo oxidasa inactivada.
Por lo tanto, generalmente a 2.5 a 3 atmósferas absolutas durante 90 a 120 minutos, se considera el tratamiento de elección para aquellos que presentan síncope, coma o convulsiones; un déficit neurológico focal; o carboxihemoglobina mayor que 25% (15% en el embarazo).
En teoría, el oxígeno normobárico debería ser el tratamiento para los pacientes menos severamente envenenados, reservándose la oxigenoterapia hiperbárica para las intoxicaciones graves. Sin embargo, hay problemas con esta política:
- Los niveles de carboxihemoglobina no se correlacionan con la gravedad clínica del envenenamiento por monóxido de carbono.
- No existe una escala de gravedad universalmente aceptada para el envenenamiento por monóxido de carbono, aunque la pérdida de conciencia y los déficits neurológicos generalmente indican una intoxicación grave.
- Todas las víctimas de intoxicación por monóxido de carbono están en riesgo de sufrir secuelas neuropsicológicas retrasadas.
Por lo tanto, en general, el siguiente enfoque es apropiado:
- Los pacientes con presunta intoxicación por monóxido de carbono deben recibir oxígeno al 100%.
- Los pacientes con intoxicación grave deben recibir oxígeno hiperbárico independientemente del nivel de carboxihemoglobina.
- Las mujeres embarazadas deben ser tratadas con oxígeno hiperbárico independientemente de los signos y síntomas.
- En pacientes con grados menores de intoxicación, se recomienda una evaluación cuidadosa antes de decidir que la terapia adecuada es oxígeno al 100% normobárico durante más de 6 horas.
La administración de más de un ciclo de oxígeno hiperbárico para quienes permanecen en coma es controvertida.
Hay varias consideraciones prácticas porque no todas las instalaciones de tratamiento, por ejemplo, las salas de emergencia de los hospitales, pueden medir carboxihemoglobina o administrar oxígeno hiperbárico.
Por ejemplo, en un estudio reciente, solo el 44% de los hospitales de agudos tenían la capacidad de medir la carboxihemoglobina.
El oxígeno hiperbárico es 100% de oxígeno a dos o tres veces la presión atmosférica a nivel del mar. La tensión de oxígeno en las arterias aumenta a aproximadamente 2000 mm Hg y la de los tejidos a casi 400 mm Hg.
La presión se expresa en múltiplos de la presión atmosférica, que es 1 a nivel del mar. A nivel del mar, la concentración de oxígeno en la sangre es de 0.3 mL/dL. Con 100% de oxígeno a presión ambiente (normobárica), la cantidad de oxígeno disuelto en la sangre aumenta cinco veces a 1,5 ml/dL.
A 3 atmósferas, el contenido de oxígeno disuelto alcanza 6 ml/dL. El oxígeno hiperbárico disminuye la formación de burbujas en la sangre y reemplaza los gases inertes con oxígeno, que los tejidos absorben y utilizan rápidamente.
El oxígeno hiperbárico puede ser bactericida o bacteriostático, o puede suprimir la producción de toxinas, aumentando la resistencia de los tejidos contra las infecciones.
El oxígeno hiperbárico es más efectivo que el oxígeno normobárico en la promoción de la formación de colágeno y la angiogénesis y, por lo tanto, puede facilitar la curación de heridas.
El oxígeno hiperbárico inhibe la adherencia de los neutrófilos a las paredes de los vasos isquémicos, lo que disminuye la producción de radicales libres, la vasoconstricción y la destrucción del tejido.
El oxígeno hiperbárico generalmente se administra en una cámara de monoplaza o, con menor frecuencia, en una cámara multiocupante. La duración de un solo tratamiento para el envenenamiento por monóxido de carbono es de aproximadamente 45 minutos.
El oxígeno hiperbárico con presiones de oxígeno de hasta 3 atmósferas durante un máximo de 120 minutos es seguro.
Los efectos adversos incluyen miopía reversible, cataratas, síntomas traqueobronquiales, ataques autolimitados y barotraumas en el oído medio, senos craneales y, rara vez, dientes o pulmones.
La claustrofobia puede ser un problema en las cámaras de monoplaza. A pesar de los resultados contradictorios de la literatura sobre el efecto del oxígeno hiperbárico versus oxígeno normobárico.
Tibbles y Edelsberg determinaron que los pacientes con intoxicación grave por monóxido de carbono deberían recibir al menos un tratamiento de oxígeno hiperbárico de 2.5 a 3.0 atmósferas porque esta terapia es el método más rápido de tratamiento de los efectos potencialmente reversibles que amenazan la vida.
El tratamiento de un paciente con intoxicación por monóxido de carbono no debe basarse únicamente en los niveles de carboxihemoglobina. Deben tenerse en cuenta las manifestaciones clínicas, los niveles de carboxihemoglobina y, lo que es más importante, el historial médico subyacente del paciente.
En pacientes con sospecha de envenenamiento por monóxido de carbono, se debe administrar oxígeno al 100% inmediatamente con una máscara.
El objetivo es aumentar la presión de los niveles de oxígeno arterial, disminuir la vida media del monóxido de carbono y facilitar su disociación de la hemoglobina, lo que permite que el oxígeno se adhiera a los sitios de unión liberados.
Se debe proporcionar reposo estricto, ya que disminuye la demanda y el consumo de oxígeno. Los pacientes con dificultad respiratoria y disminución del nivel de conciencia deben ser intubados y ventilados.
Se deben realizar radiografías de tórax, niveles de lactato en sangre y gases arteriales en el departamento de emergencias. La cefalea mejoró antes del tratamiento con oxígeno hiperbárico en un 72%, resolviéndose por completo en un 21%.
De aquellos con dolor de cabeza residual, el dolor mejoró con oxígeno hiperbárico en el 97%, resolviéndose por completo en el 44%.
Aunque las muertes por envenenamiento por monóxido de carbono han disminuido en los Estados Unidos en los últimos años, la carga total, incluidos los casos fatales y no mortales, no ha cambiado significativamente.
Juurlink et al. analizaron los datos disponibles de seis ensayos controlados aleatorios que incluyeron adultos no gestantes agudamente envenenados con monóxido de carbono.
A 1 mes de seguimiento después del tratamiento, los síntomas posiblemente relacionados con el envenenamiento por monóxido de carbono estaban presentes en 34.2%, no en aquellos tratados con oxígeno hiperbárico, en comparación con 37.2% no tratados con oxígeno hiperbárico.
No encontraron pruebas de que el uso no seleccionado de oxígeno hiperbárico en el tratamiento del envenenamiento agudo por monóxido de carbono reduzca la frecuencia de los síntomas neurológicos en 1 mes.
Debido a la evidencia insuficiente, recomiendan una mayor investigación para definir el papel del oxígeno hiperbárico en el tratamiento del envenenamiento por monóxido de carbono.
Cinco años más tarde, el mismo grupo examinó la evidencia de la efectividad del oxígeno hiperbárico para la prevención de secuelas neurológicas en pacientes con intoxicación aguda por monóxido de carbono.
Cuatro de seis ensayos no encontraron beneficios del oxígeno hiperbárico para la reducción de las secuelas neurológicas, mientras que otros dos encontraron beneficios para el oxígeno hiperbárico.
Los autores concluyen que los ensayos aleatorizados existentes no han podido establecer la reducción de las secuelas neurológicas con la administración de oxígeno hiperbárico a pacientes con intoxicación por monóxido de carbono.
Se requiere una estrecha monitorización del pH sérico y de los niveles de ácido láctico, ya que el metabolismo anaeróbico en presencia de hipoxia tisular genera acidosis láctica. La acidosis por debajo de 7.15 pH debe tratarse con bicarbonato de sodio.
Se debe tener precaución con la administración de bicarbonato de sodio porque el dióxido de carbono, un subproducto de su metabolismo, podría provocar acidosis respiratoria y debe eliminarse con la ventilación adecuada.